ДИАЗОУКСУСНЫЙ ЭФИР
(этиловый эфир диазоуксусной к-ты) N2CHCOOC2H5, мол. м. 114,1; желтая вязкая жидкость; т. пл. -22°С, т. кип. 140-141 °С; d420 1,0921; nD20 1,4616; раств. в этаноле, диэтиловом эфире, бензоле, трудно - в воде.
Д. э. широко используется в орг. синтезе; во мн. р-циях промежуточно образуются диазоний-катион +N2СН2СООС2Н5 или этоксикарбонилкарбен :СНСООС2Н5. С галогеноводородными к-тами и галогенами Д.э. дает соотв. моно- и дигалогенуксусные эфиры, напр.:
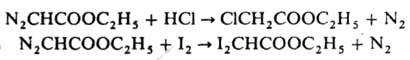
С водой, спиртами, карбоновыми к-тами реагирует по схеме:
N2CHCOOC2H5 + ROH : ROCH2COOC2H5 + N2
(R = H, Alk, Ac). Присоединение Д. э. по кратным связям и внедрение :СНСООС2Н5 по простым связям используется для расширения цикла ароматич. соединений и циклич. кетонов и получения производных циклопропана, напр.:
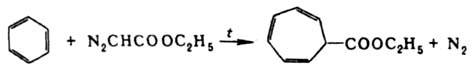
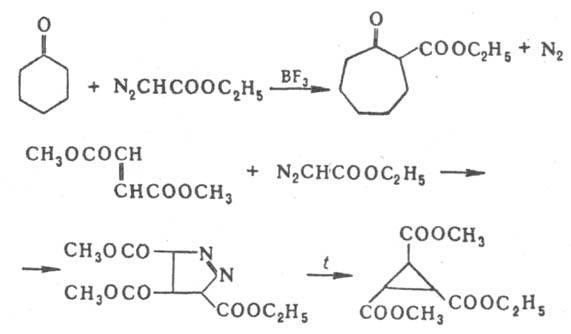
С нитрилами Д.э. дает оксазолы:
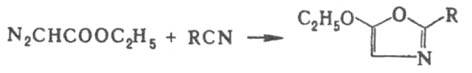
При взаимод. с конц. NH3 образует глицин, аспарагиновую к-ту и их амиды. При нагр. с порошком Си дает диэтилфумарат, а при обработке щелочью - производное сим-тетразина.
Направление восстановления Д.э. зависит от используемого реагента:
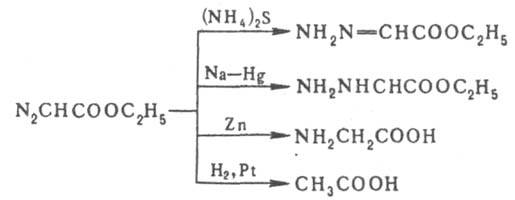
Получают Д.э. р-цией гидрохлорида этилового эфира глицина с азотистой к-той:
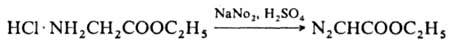
При действии конц. H2SO4 и НСl, а также при нагр. в недостаточно очищенном виде Д. э. разлагается со взрывом. Токсичен.
Лит.: Физер Л., Физер М., Реагенты для органического синтеза, пер. с англ., т. 1, М., 1970, с. 249-50; Общая органическая химия, пер. с aнгл., т. 3, М., 1982,с. 306; там же, т. 4, М., 1983, с. 266. И. В. Хвостов.
|